脂蛋白(a)升高的功能医学干预策略
脂蛋白(a) [Lp(a)] 是一种独立的、遗传性较强的血脂指标,其水平升高与动脉粥样硬化性心血管疾病 (ASCVD) 风险显著相关,包括心肌梗死、缺血性卒中和主动脉瓣狭窄等。与LDL-C(“坏”胆固醇)不同,Lp(a) 的水平主要由基因决定,受饮食和生活方式的影响较小。
功能医学(Functional Medicine)强调个体化治疗和寻找疾病的根本原因,虽然Lp(a)主要受遗传影响,但在功能医学的框架下,对Lp(a)的干预会更侧重于降低整体心血管风险和优化身体的整体功能,以弥补Lp(a)升高带来的潜在危害。
根本认识:脂蛋白a的结构与风险
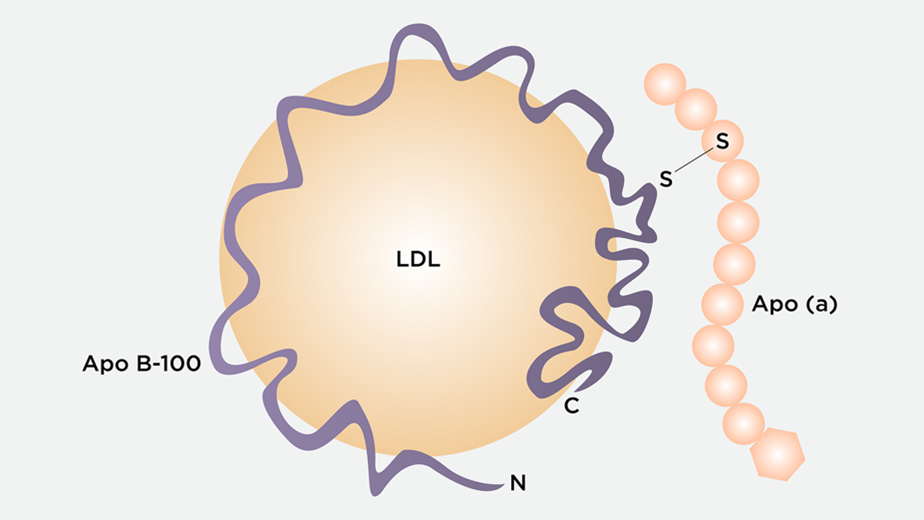
Lp(a) 由两个主要部分构成:
① Lp(a)结构类似于LDL,apoB-100是LDL的主要蛋白部分。
② 外层附着一个apo(a)蛋白,是一种富含半胱氨酸和赖氨酸结构域的蛋白,apo(a)具有与纤溶酶原结构相似的区域,阻碍纤溶系统清除血栓,促进动脉粥样硬化与血栓形成。

LP(a)升高的原因
Lp(a)升高的原因可分为原发性(遗传性)和继发性(环境或代谢相关)两大类。多数人的Lp(a)水平终身保持稳定,但某些生理或病理因素可加重其升高趋势或放大其致病性。
Lp(a)升高的主要原因
| 类型 | 原因 | 说明 |
| 原发性(遗传性) | LPA基因多态性/突变 | 是最主要原因,决定90%以上Lp(a)浓度,尤其是 apo(a)结构越短,Lp(a)越高、风险越大 |
| 生理性 | 绝经/年龄增长 | 雌激素下降后,Lp(a)自然升高,尤其在女性明显;老年人也常见升高 |
| 内分泌/代谢性 | 甲状腺功能减退、糖尿病、胰岛素抵抗 | 会加重脂蛋白代谢紊乱,影响Lp(a)清除与功能 |
| 慢性炎症状态 | 高CRP、慢性感染、自身免疫疾病 | 促发Lp(a)氧化、与血管壁结合增强 |
| 药物因素 | 雌激素撤药、糖皮质激素、抗病毒药物等 | 部分药物影响LPA表达或脂蛋白代谢路径 |
| 饮食/生活方式不良 | 高反式脂肪、高果糖、缺乏抗氧化剂、抽烟等 | 加重氧化型Lp(a)毒性,少数人饮食可小幅升高Lp(a)浓度 |
| 肾功能异常 | 轻度肾病/蛋白尿状态 | 肾脏为Lp(a)清除器官之一,功能下降时可升高其浓度 |
| 遗传性脂蛋白代谢病 | 如家族性高胆固醇血症(FH) | 常合并Lp(a)升高,加倍心血管风险 |
遗传性Lp(a)升高
① LPA基因编码apo(a),apo(a)由重复性的KIV(kringle IV)结构域构成。
② 重复次数越少 → apo(a)分子越小 → 合成速度越快 → Lp(a)浓度越高(>50mg/dL通常为风险界限)。
③ 常见高风险基因型包括:rs10455872、rs3798220。
遗传决定你“生成了多少Lp(a)”,但你仍能决定“这些Lp(a)是否致病”。
检测和个体化评估
| 基因检测:LPA基因多态性(如rs10455872和rs3798220)可以预测Lp(a)水平和心血管风险,了解根源机制与干预方向。
| 营养基因组评估:如MTHFR(叶酸代谢)、APOE(脂代谢)、CETP等基因,指导更个性化的干预。
| 功能医学检测建议:
- Lp(a)
- hs-CRP:表明体内炎症活跃,Lp(a)更易氧化、沉积于动脉壁
- 同型半胱氨酸:与Lp(a)协同损伤血管内皮、促进血栓形成
- ApoB、LDL-P(颗粒数量)与Lp(a)协同,增加“LDL颗粒数+毒性”
- 脂溶性抗氧化物:如缺乏则加速Lp(a)氧化,增强血管粘附力
- 甲基化代谢
- 甲状腺功能:TSH/FT3/FT4,排除内分泌相关升高
- 肾功能(eGFR、尿蛋白),判断清除能力是否下降
功能医学干预脂蛋白(a)的策略
鉴于Lp(a)的特殊性,目前尚无特定的药物可以直接大幅度降低Lp(a)水平,并同时被证明能带来心血管事件的额外获益。因此,功能医学的干预更注重以下几个方面:
1
全面评估心血管风险
功能医学会综合评估患者的整体心血管风险因素,包括:
- 其他血脂指标:严格控制LDL-C、甘油三酯等其他“坏”胆固醇,并提升HDL-C(“好”胆固醇)。
- 炎症指标:检测并管理高敏感C反应蛋白 (hs-CRP) 等炎症标志物,因为Lp(a)本身也具有促炎作用。
- 血糖稳态:评估胰岛素抵抗、血糖波动等情况,这些都与心血管疾病风险密切相关。
- 血压管理:优化血压水平。
- 同型半胱氨酸:监测同型半胱氨酸水平,高水平可能增加心血管风险。
- 氧化应激:评估体内的氧化应激水平,因为Lp(a)易受氧化修饰,产生促炎物质
2
优化生活方式干预
尽管生活方式对Lp(a)本身的水平影响有限,但它是降低整体心血管风险的重要基石。功能医学会强调:
★ 健康饮食
饮食对Lp(a)的可能影响一些研究还是探讨了特定饮食模式或营养素与Lp(a)水平之间潜在的关系。值得注意的是,目前还没有哪种特定的饮食方式被证实能大幅度、持续地降低Lp(a)水平,并带来显著的心血管获益。
脂肪的种类
♦ 饱和脂肪和反式脂肪:有些研究发现,摄入较多的饱和脂肪(如红肉、加工肉类、黄油、某些植物油)和反式脂肪(多存在于加工食品、油炸食品中)可能会轻微升高Lp(a)水平。同时,这两种脂肪本身就对心血管健康不利,会升高LDL-C并增加炎症风险。所以,无论Lp(a)高不高,都建议限制它们的摄入。
♦ 不饱和脂肪:包括单不饱和脂肪(如橄榄油、牛油果、坚果)和多不饱和脂肪(如鱼油中的Omega-3脂肪酸,以及植物油中的Omega-6脂肪酸)。富含这些健康脂肪的饮食通常被认为对心血管有益。虽然它们对Lp(a)的直接影响不大,但可能通过降低甘油三酯、抗炎和改善血管功能来间接支持心血管健康。
碳水化合物与膳食纤维
♦精制碳水化合物与糖:过量摄入精制碳水化合物和糖(如白米饭、白面包、含糖饮料、糕点)可能导致胰岛素抵抗和甘油三酯升高,这些都与心血管风险相关。目前没有确凿证据表明它们直接影响Lp(a),但为了整体心血管健康,建议减少它们的摄入。
♦ 膳食纤维:特别是可溶性膳食纤维(如燕麦、豆类、水果、蔬菜中的纤维),能有效降低LDL-C。虽然它对Lp(a)的直接影响不明确,但富含纤维的饮食对心血管系统非常有益。
蛋白质
蛋白质来源与Lp(a)的关系研究相对较少,也没有明确的结论表明某种蛋白质能显著影响Lp(a)水平。选择瘦肉蛋白、植物蛋白(豆类、坚果)通常被认为是健康的选择。
维生素与矿物质
♦ 烟酸(维生素B3):烟酸是少数被认为能降低Lp(a)的营养素。在一些研究中,大剂量烟酸可以将Lp(a)降低15%至25%。然而,大型临床试验结果显示,尽管烟酸能降低Lp(a)和LDL-C,但它并没有额外降低心血管事件的风险,反而可能增加副作用(如潮红、血糖升高)的风险。因此,目前医生不推荐为了降低Lp(a)而常规使用烟酸。
♦ 维生素C:有一种理论认为,维生素C在血管健康中起作用,一些观点认为其可能影响Lp(a)在血管壁的沉积。但这主要停留在假说阶段,缺乏高质量的临床证据来支持维生素C能直接降低Lp(a)或减轻其危害。
| 重点:饮食在Lp(a)管理中的作用——既然饮食对Lp(a)的直接影响有限,那么对于Lp(a)升高的人群来说,饮食的作用体现在哪里呢?
| 降低整体心血管风险:即使Lp(a)本身难以通过饮食显著改变,但通过健康的饮食模式,我们可以优化其他心血管风险因素,从而降低总体的心血管疾病风险。例如:降低LDL-C和甘油三酯,改善血压和血糖控制,减轻全身炎症和氧化应激。
| 推荐的饮食模式:抗炎+控糖+清脂
- 地中海饮食模式:富含蔬菜、水果、全谷物、健康脂肪(如橄榄油、坚果、种子)和鱼类,限制红肉、加工食品和糖。这种饮食模式有助于降低炎症、改善血脂谱和整体心血管健康。
- 足量膳食纤维:有助于降低胆固醇、稳定血糖。
- 抗氧化食物:摄入富含抗氧化剂的食物(如深色浆果、绿叶蔬菜),以减少氧化应激。
★ 饮食总结 ★
| 饮食策略 | 具体建议 | 原因与机制 |
| 地中海饮食或抗炎饮食 | 多蔬果、橄榄油、坚果、深海鱼 | 富含抗氧化物与Omega-3,降低炎症与氧化Lp(a) |
| 高膳食纤维饮食 | 豆类、亚麻籽、糙米、糙麦 | 降低胆固醇、改善肠道菌群,有助调节脂蛋白代谢 |
| 富含抗氧化营养的食物 | 蓝莓、绿茶、姜黄、洋葱、大蒜 | 中和Lp(a)引发的自由基损伤 |
| 限制高糖/高果糖食物 | 含糖饮料、甜点、果糖浆 | 高血糖→AGEs生成↑→血管氧化损伤↑ |
| 限制反式脂肪与精制油脂 | 炸物、人造黄油、糕点 | 反式脂肪可升高Lp(a),加重动脉粥样硬化 |
对于Lp(a)偏高的人群,饮食的重点不应放在“如何直接降低Lp(a)”上,而应放在“如何通过优化整体饮食结构来降低心血管疾病的总风险”。这意味着选择健康的脂肪、全谷物、足量蔬菜水果,限制加工食品、高糖食品和不健康的脂肪。如果您被告知Lp(a)水平偏高,请务必咨询您的医生或注册营养师,他们会根据您的具体情况提供个性化的饮食建议和风险管理方案。
★ 规律运动
改善血管与脂质环境。适度有规律的体育锻炼对心血管健康至关重要,有助于改善血脂、血压、血糖和减轻体重。
| 类型 | 建议 | 好处 |
| 有氧运动 | 快走、游泳、骑行,每周150–300分钟 | 改善胰岛素敏感性、降低炎症与内皮损伤 |
| 抗阻训练 | 2–3次/周 | 增加肌肉量,增强代谢适应性 |
| 高强度间歇(适合者) | 1–2次/周 | 提升线粒体功能与代谢柔韧性 |
| 日常活动增加 | 避免久坐,每小时起身走动 | 维持代谢激活状态、减少胰岛素刺激 |
★ 体重管理:维持健康的体重有助于降低多种心血管风险因素。
★ 压力管理:降低神经-内分泌驱动的炎症,慢性压力可能影响心血管健康,功能医学会通过冥想、瑜伽、呼吸练习等方法来帮助患者管理压力。
| 方法 | 推荐方式 |
| 冥想、正念呼吸 | 每天10–20分钟,配合腹式呼吸 |
| 自然接触 | 每周接触自然环境≥2小时 |
| 情绪表达 | 写情绪日记、疗愈谈话、艺术表达 |
| 规律作息 | 每晚睡足7–8小时,避免熬夜 |
| HRV生物反馈训练 | 如设备Biofeedback等 |
★ 充足睡眠:保证高质量的睡眠对整体健康和心血管功能至关重要。
| 睡眠建议 | 原因 |
| 保持稳定的入睡时间 | 稳定生物钟,降低夜间交感激活 |
| 避免过晚进食与高糖摄入 | 减少夜间高胰岛素影响脂代谢 |
| 睡前屏幕关闭 ≥1小时 | 降低褪黑素抑制,改善深睡眠 |
| 有睡眠障碍者检测HRV或OSA | 睡眠呼吸暂停(OSA)与Lp(a)升高相关 |
★ 戒烟限酒: 戒烟是降低心血管风险最有效的措施之一。烟增加Lp(a)氧化速度,显著提升心梗风险;酒精小剂量红酒或无酒精红葡萄提取物可提供抗氧化多酚,但不建议借酒护心。
3
个体化营养补充
在功能医学中,可能会根据患者的具体情况和检测结果,考虑以下营养补充剂,但其对Lp(a)的直接影响和临床获益仍需更多研究:
- 烟酸(Niacin):曾被认为可以降低Lp(a),但最新研究表明,虽然它可以降低Lp(a)水平,但并未额外降低心血管事件风险,甚至可能产生不利副作用,因此不作为常规推荐。
- PCSK9抑制剂:这类药物在显著降低LDL-C的同时,也能降低Lp(a)水平约25%,但其降低心血管事件风险的主要机制是降胆固醇本身。
- 鱼油(Omega-3 脂肪酸):可能有助于降低甘油三酯和改善炎症,对整体心血管健康有益。
- 其他抗氧化剂和抗炎补充剂:如辅酶Q10、白藜芦醇、姜黄素等,可能有助于减轻氧化应激和炎症,从而间接支持心血管健康。
Lp(a) 与营养代谢的关键联系
| 营养 | 影响机制 | 与Lp(a)关系 |
| 烟酸(Niacin) | 调节肝脏脂蛋白合成,抑制apo(a)表达 | 高剂量烟酸可显著降低Lp(a)(达20-30%),但易引起潮红、肝毒性等不良反应,需在医生指导下使用 |
| 甲基化营养素(叶酸、B12、B6、甜菜碱) | 参与一碳代谢,影响LPA基因甲基化及肝脏脂蛋白合成 | 甲基化异常可能促进Lp(a)表达;适量补充可改善代谢环境,但对Lp(a)降低有限 |
| 维生素C | 支持血管胶原合成、抗氧化 | 不直接降低Lp(a),但可减少其氧化损伤,缓解动脉粥样硬化风险;有学者建议联合赖氨酸使用 |
| 赖氨酸 | 竞争性抑制Lp(a)与血管壁结合 | Linus Pauling理论认为其可阻断Lp(a)对血管壁的粘附,降低动脉斑块形成可能 |
| Omega-3脂肪酸(EPA/DHA) | 降低炎症、改善脂质代谢 | 不能显著降低Lp(a)水平,但可改善其致病环境(炎症、血管损伤) |
| 抗氧化剂(CoQ10、硒、NAC、维生素E) | 抑制氧化应激,保护内皮功能 | Lp(a)易被氧化,促进动脉损伤;营养抗氧化剂可降低氧化型Lp(a)的危害 |
| 左旋精氨酸(L-Arginine) | 促进NO合成,改善血管功能 | 降低Lp(a)介导的血管收缩与损伤风险 |
| 硫辛酸、谷胱甘肽 | 增强线粒体与抗氧化系统 | 改善内皮功能、抵御Lp(a)氧化损伤 |
| 维生素D | 调节免疫与炎症 | 可能通过减少炎症间接改善Lp(a)所致动脉硬化,但无证据显示可直接影响Lp(a) 水平 |
营养素调节(降低Lp(a)或减少其损伤性)
| 营养素 | 推荐剂量/建议 |
| 烟酸(Niacin,维生素B3) | 1–3g/天(需在医生指导下使用) |
| 维生素C | 1–3g/天(分次服用,缓解胃肠刺激) |
| 赖氨酸 | 2–5g/天,搭配维生素C |
| 左旋精氨酸(L-Arginine) | 2–6g/天(注意是否合并病毒感染) |
| Omega-3脂肪酸(EPA/DHA) | 每天EPA+DHA总量 ≥ 2g |
| CoQ10(辅酶Q10) | 100–300mg/天 |
| NAC(N-乙酰半胱氨酸) | 600–1800mg/天 |
| 硫辛酸(ALA) | 300–600mg/天 |
肝脏与甲基化支持(减少合成、改善代谢)
- 支持肝脏解毒:如使用乳蓟草、胆汁流支持配方、硫代葡萄糖素等植物营养素。
- 改善甲基化通路(可能影响Lp(a)合成):使用活性叶酸(5-MTHF)、维生素B12(甲钴胺)、B6(P5P)、胆碱、甜菜碱(TMG)。
减少氧化型Lp(a)与炎症反应
- 抗氧化营养素:维生素E、硒、谷胱甘肽、植物多酚(如白藜芦醇、绿茶提取物)。
- 调节慢性炎症:检测hs-CRP、氧化LDL、MPO(髓过氧化物酶),并用营养或草本抗炎干预。
4
药物干预(医生指导下)
对于Lp(a)水平显著升高且心血管风险较高的患者,即便Lp(a)难以直接药物干预,医生仍会积极使用其他已被证实能降低心血管事件的药物,例如:
- 他汀类药物:尽管他汀类药物对Lp(a)水平影响不大甚至可能略微升高,但它们能有效降低LDL-C,显著降低心血管事件风险,因此仍是基础治疗。
- PCSK9抑制剂:对于高危患者,如果他汀类药物无法使LDL-C达标,或存在他汀不耐受,PCSK9抑制剂是重要的选择。
5
新型疗法(研发中)
目前有一些针对Lp(a)的新型药物正在研发中,例如靶向Apo(a) mRNA的反义寡核苷酸(如Pelacarsen),这些药物在临床试验中显示出显著降低Lp(a)水平的潜力,有望在未来为Lp(a)升高的患者提供更有效的治疗选择。
干预效果追踪建议
| 项目 | 周期 | 目的 |
| Lp(a) | 每6–12月 | 判断基线水平与遗传风险 |
| hs-CRP | 每3–6月 | 追踪慢性炎症 |
| ApoB / LDL-P | 每3–6月 | 追踪动脉风险指标 |
| HRV(心率变异性) | 每月(如可测) | 监控自主神经系统压力反应 |
| 血压/血糖/体脂 | 每周–每月 | 综合代谢状态追踪 |
Lp(a)升高的生活方式干预四大核心目标
抗氧化:降低氧化Lp(a)生成
抗炎:降低hs-CRP、MPO等炎症指标
血管修复:改善内皮功能,阻断粘附与沉积
代谢优化:控制胰岛素、脂肪毒性,改善代谢环境
总结
脂蛋白(a)的干预是一个复杂的问题,尤其是考虑到其遗传特性。Lp(a)的浓度主要由基因决定,但它是否致病,取决于炎症水平、代谢状态和生活方式。功能医学的干预并非替代传统医学治疗,而是一种补充和整合的方法。任何针对Lp(a)的干预措施都应在专业医生(尤其是心血管专科医生或功能医学医生)的指导下进行,并定期监测相关指标。 不要自行诊断和治疗,以免延误病情或造成不良后果。





发表回复